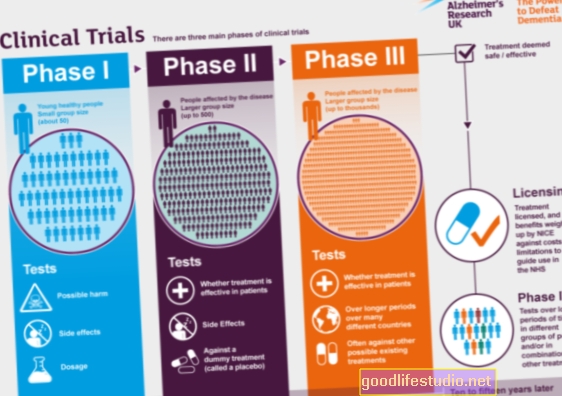
Наркотик Альцгеймера провалює клінічні випробування
Елі Ліллі оголосила, що зупиняє розробку препарату, який називається семагацестат, інгібітор ферменту гамма-секретази, що продукує бета-амілоїдний білок, після попередніх результатів двох великих плацебо-контрольованих досліджень, що не показали жодної користі від лікування.
"Це не сповільнило прогресування захворювання і було пов'язане з погіршенням клінічних показників пізнання та здатності виконувати повсякденну діяльність", - йдеться у прес-релізі Lilly.
Загалом у випробуваннях взяли участь понад 2600 учасників із хворобою Альцгеймера легкої та середньої тяжкості. Пацієнти, які отримували препарат, зазнали більшого зниження цих показників, ніж у пацієнтів із групами плацебо.
Ліллі заявила, що доручила слідчим сайту якнайшвидше припинити дозування пацієнтів, але продовжувати слідкувати за учасниками принаймні протягом шести місяців для збору оцінок когнітивних функцій та даних про безпеку.
"Ці додаткові наступні візити допоможуть відповісти на низку важливих питань, зокрема, чи продовжуватимуться розбіжності між пацієнтами, які отримували семагацестат, і тими, хто отримував плацебо, після припинення застосування семагацестату", - зазначила компанія.
Два судові процеси розпочались у 2008 році; один повинен був працювати до червня 2011 року, а другий - до березня 2012 року.
Ліллі також зупиняє інші, менші, короткострокові дослідження семагацестату.
Препарат є останнім антиамілоїдним агентом, який не зазнав успіху на пізніх стадіях плацебо-контрольованих випробувань, ставлячи більше сумнівів у тому, чи може цей підхід коли-небудь спрацювати при встановленій хворобі Альцгеймера.
Негативні клінічні результати також були виявлені для таренфлурбілу, латрепірдину (димебону) та бапінеузумабу, які націлені на вироблення бета-амілоїдного білка, або липкі бляшки, які утворюються при зміні форми розчинного бета-амілоїду на волокнисті та нерозчинні.
Але розробка бапінеузумабу триває, попередні дані ПЕТ-сканування вказують на те, що препарат успішно розщеплює амілоїдні бляшки у пацієнтів з хворобою Альцгеймера за призначенням. Зараз у громаді Альцгеймера з нетерпінням чекають клінічних результатів дослідження фази III.
Випробування Lilly на семагацестаті також включали сканування ПЕТ для вимірювання впливу на наліт нальоту. Оголошення компанії не включало ці результати; прес-секретар Lilly заявив, що дані ПЕТ все ще сліпі та не будуть доступні для аналізу щонайменше шість місяців.
Ці дані можуть мати вирішальне значення при визначенні того, чи є бета-амілоїд цінною мішенню для препаратів Альцгеймера, а також те, що пішло не так із семагацестатом.
Висновок про те, що лікування семагацестатом зменшило накопичення нальоту, але не показало клінічної користі, може свідчити про те, що такий підхід не буде працювати у пацієнтів із встановленими симптомами.
Ліллі підкреслила, що вона ще не відмовляється від бета-амілоїду як мішені. Компанія продовжує розробку антиамілоїдного моноклонального антитіла, соланезумабу, з двома випробуваннями III фази.
Джерело: MedPage Today